Farefull spleising - en ny måte å tenke om det skadelige huntingtinproteinet
Forskere oppdager en ny måte skadelige fragmenter av huntingtin-proteinet blir dannet i nerveceller.
Av Dr Tamara Maiuri 5. februar 2014 Redigert av Professor Ed Wild Oversatt av Kristin Iversen Opprinnelig publisert 6. mai 2013
Forskere gjør en stor innsats for å finne ut nøyaktig hvordan det forlengede genet for Huntingtons sykdom (HS) forårsaker skade. Arbeid som nylig er gjennomført av en britisk forskergruppe, har avdekket et nytt spor som kan hjelpe til å løse mysteriet. Det viser seg at feilaktig behandling av “huntingtinoppskriften” medfører dannelse av et kort, skadelig fragment av huntingtinproteinet.
Kokeboka, oppskriften og kirsebærpaien
Huntingtons sykdom er forårsaket av en uønsket forlengelse av huntingtin-genet. Men genene består kun av DNA, og det er det forlengede proteinet, huntingtin, som er årsaken til problemene. Men hvordan kommer vi fra DNA til protein? - Jo, via et mellomliggende budbringer-molekyl som heter RNA.

Det kan hjelpe å forestille seg en bestemor som er litt for ivrig til å passe på oppskriftene sine, og holder kokeboka si innelåst i et hvelv, slik at den ikke kommer til skade på kjøkkenet. Alle som vil å lage den berømte kirsebærpaien hennes, må gå inn i hvelvet, ta en fotokopi av oppskriften, og så ut i kjøkkenet igjen for å finne fram ingrediensene.
Omlag på samme måten passer cellene på DNA'et vårt inne i cellekjernen. RNA-kopier av genene lages i cellekjernen, transporteres ut i cytoplasma, hvor de så “oversettes” til et protein. RNA-meldinger fungerer som oppskrifter som forteller cellene akkurat hvilke ingredienser som må brukes for å lage det aktuelle proteinet.
I de tilfellene huntingtingenet er forlenget, vil RNA-kopien også være forlenget. Sluttproduktet, huntingtinproteinet, vil inneholde for mange “ingredienser”, og vil derfor formes feil. Selv om man vet at denne ekspansjonen forårsaker Huntingtons sykdom, forstår man fortsatt ikke nøyaktig hvordan det forlengede proteinet skader nervecellene.
For å gjøre en lang historie kort
Huntingtingenet er svært langt; et av de lengste genene vi har, og er oppskriften på et svært stort protein. Den unormale, ekspanderte delen befinner seg helt i starten av genet, - i oppskriftens første linje kan vi si.
En ting man har merket seg, er at man i hjernecellene både hos Huntington-pasienter og i musemodellene man bruker i forskningen, finner svært korte versjoner av huntingtinproteinet; kun de første fem prosentene eller så.
Så hvordan oppstår disse korte fragmentene? Fram til nå har man trodd at spesielle delingsproteiner delte opp huntingtinproteinet i små biter av huntingtin.
Fragmenter som inneholder den unormale forlengelsen er skadelige for hjernecellene. Forskere, ledet av professor Gill Bates ved King’s College London, foreslo at disse fragmentene kan oppstå på en annen måte, og at det foregår på det stadiet hvor RNA-kopien blir laget i cellekjernen.
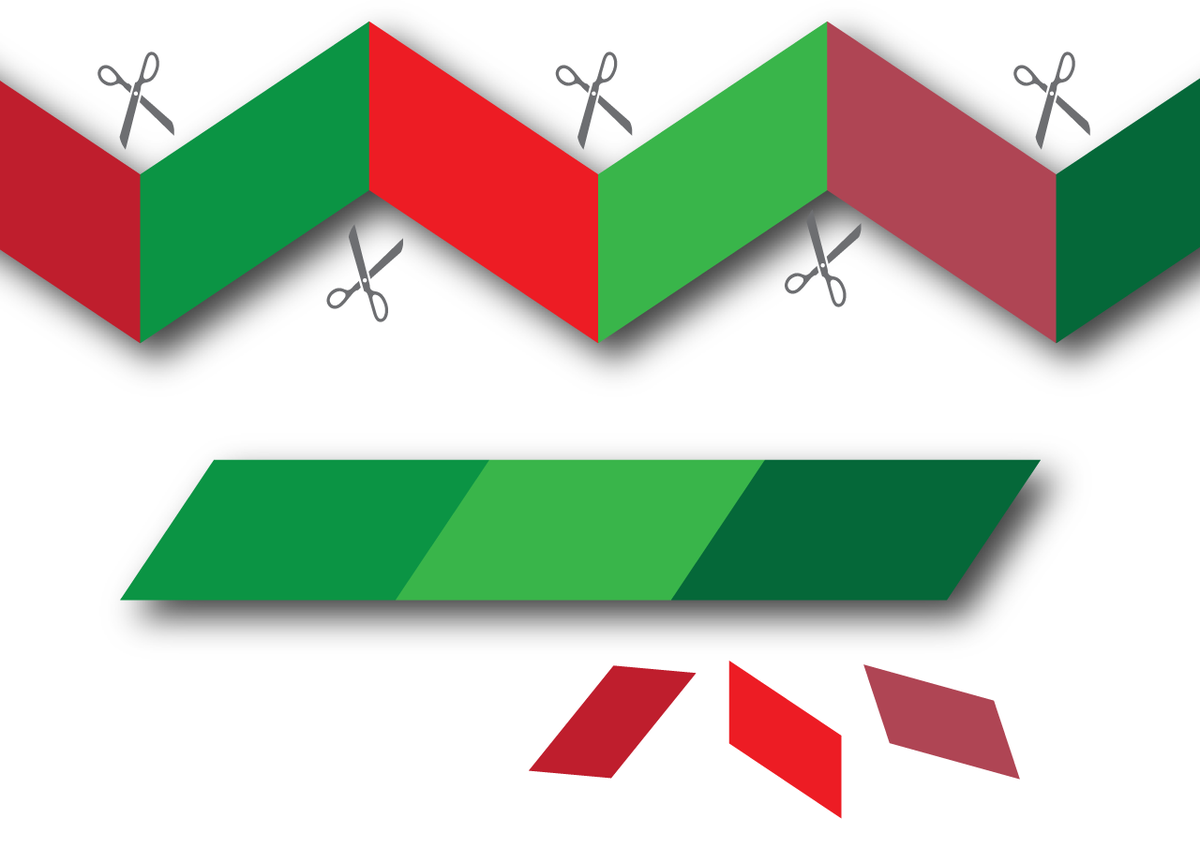
Klipping og liming
Som vi husker består genene av DNA, som blir kopiert over til RNA, som så blir “oversatt” til protein. Enkelt, ikke sant? Men som ved de fleste prosesser i naturen, finnes det et ekstra, mer komplekst nivå man må ta i betraktning.
«Spleising, hvor ikke-kodende sludder blir fjernet fra RNA-meldingen, går galt ved Huntingtons sykdom. »
Gener inneholder både kodende og ikke-kodende områder; organisert i sekvenser som zebrastriper. Bare de kodende områdene ender opp som proteiner, mens de ikke-kodende områdene blir fjernet.
I prosessen med å kopiere DNA til RNA, blir det først laget en kopi av hele genet, og så blir de ikke-kodende områdene fjernet fra RNA'et, i en prosess som kalles spleising.
Hvis vi benytter oss av analogien med bestemors kokebok igjen, kan vi forestille oss dette som at kokeboka har linjer med uforståelig språk, som kommer mellom linjene med instruksjoner. Hele oppskriften, inkludert det uforståelige, blir kopiert inne i hvelvet. Så blir kopien klippet opp og satt sammen igjen, uten de uforståelige linjene, før den kommer ut i kjøkkenet.
Så hva er det nye?
Ved å studere mus, har Bates’ team funnet ut at det er i “spleisefasen”, hvor det ikke-kodende området blir fjernet fra RNA'et, at det kan gå galt. Når huntingtin-RNA'et er forlenget, slik som ved Huntingtons sykdom, vil dette skje.
Hos friske mus ble det ikke-kodende området fjernet slik det skulle, og de to første kodende områdene ble spleiset sammen på riktig måte. En meningsfull melding av full lengde ble dannet.
Men i mus som har et ekspandert huntingtin-gen, ble ikke det første ikke-kodende området fjernet ordentlig. Inne i dette området ligger det en beskjed til cellen om å kutte opp dette RNA'et. Som et resultat, ble det hos de genmodifiserte musene laget en ekstra, kort RNA-budbringer, bestående kun av det første kodende området pluss deler av det ikke-kodende området.
Når denne korte RNA-meldingen blir omgjort til protein, ender musene opp med et kort fragment av huntingtin-proteinet som inneholder det ekspanderte området. Dette er akkurat det fragmentet man mener er skadelig ved HS.
Teamet så også på prøver fra mennesker med Huntingtons sykdom. Den unormale, korte RNA-budbringeren og proteinet ble funnet hos noen, men ikke hos alle. Dette kan være pga at dannelsen av de små fragmentene kan variere i ulike celler eller mellom forskjellige pasienter.
Hvordan blir spleisingen forstyrret av den ekspanderte RNA-kopien? Bates’ team viste at et protein som vanligvis har til oppgave å organisere RNA-budbringermolekyler, fester seg til det ekspanderte huntingtin-RNA'et, men ikke til normalt huntingtin-RNA. Det kan da være slik at denne prosessen forstyrrer en riktig spleising, og resulterer i den korte og feilaktige kopien av huntingtin.
Hva gjør vi med dette nye sporet?
Denne studien hjelper oss til å forstå en mulig ny måte for hvordan skadelige fragmenter av huntingtin dannes.
Våre hjerner og nerveceller er svært komplekse strukturer. Den nye mekanismen er ikke nødvendigvis den eneste måten de skadelige proteinfragmentene oppstår på. Den tradisjonelle forståelsen med kløyving er ikke utelukket pga dette nye funnet, og begge mekanismene kan være i funksjon samtidig.
I tillegg er sannsynligvis ikke de farlige fragmentene den eneste måten det forlengede huntingtinet gjør skade på.
Denne nye informasjonen er et viktig tillegg til vår kunnskap om hvordan forlenget huntingtin oppfører seg i hjernen. Og jo mer vi vet, jo bedre rustet er vi til å takle de problemene som oppstår.
Dette arbeidet kan få følger for de såkalte “gen-blokkerings-terapiene”, som tar sikte på å redusere dannelsen av huntingtinproteinet. Dette gjøres ved å merke RNA-budbringerne slik at cellene kvitter seg med dem.
Fram til nå tenkte man at alle huntingtin-RNA-budbringerne var av full lengde. Forskere må nå ta i betraktning at noe av det skadelige huntingtinet kan komme fra kortere RNA-budbringere, og som nettopp derfor ikke blir fanget opp av de aktuelle medikamentene som skal blokkere genet.
Heldigvis har vi, i flere dyremodeller av HS, allerede sett at medikamenter for gen-blokkering virker. Det er derfor klart at den nye forskningen ikke gjør den allerede kjente tilnærmingen verdiløs. Det å øke vår kunnskap, gir oss derimot nye måter å forstå hvordan genfeilen forårsaker Huntingtons sykdom, og legger “unormal spleising” til listen med mulige angrepspunkter for å løse problemet.


